【ニュース】新型コロナ感染症に対するアルテスネイトの可能性!
2021年8月12日 NHK国際ニュースより
WHOは新型コロナ感染症に対する可能性のある治療法としてアルテスネートがその一つに選ばれ世界52か国の600を超える病院で臨床試験が開始されるようです。
イベルメクチンは出荷調整がかかっており入手困難ですが当院ではアルテスネートを用いた癌治療を行っておりますので薬剤の入手が可能です。
自宅待機での重症化対策の一環としてご検討ください。
料金
| Artemix-M60 | ¥51,840(税抜) |
|---|
アルテミシニン誘導体アルテスネイトによるがん治療

アルテスネイトの抗がん効果
アルテスネイトはさまざまながん細胞に対して抗腫瘍効果を示すことが報告されています。
培養細胞や動物実験では、白血病、乳がん、肺がん、胃がん、肝臓がん、胆管がん、卵巣がん、子宮頸がん、子宮内膜がん、 骨髄腫、膵臓がん、大腸がん、脳腫瘍、前立腺がん、咽頭扁平上皮がん、口腔扁平上皮がん、悪性黒色腫などに対する抗腫瘍作用が報告されています。
臨床例での有効性を認めた症例報告も多くあります。
アルテミシニンについて
中国では古くから青高(せいこう/※高の字は、正しくは高に草冠となります)というキク科ヨモギ属の植物が、解熱剤などとして用いられてきました。
青高から分離されたアルテミシニンとその誘導体アルテスネイトは、現在マラリアの治療薬として世界中で使用されています。
そして近年、アルテミシニンに抗がん作用があることが多くの研究で明らかにされてきました。
副作用について
抗腫瘍作用を示す投与量では正常細胞に対する毒性が比較的低く、副作用が少ないと期待されています。
アルテスネイトは昔からマラリアの治療に使われていた生薬の成分で、安全性が高く副作用が軽度であるとの報告があります。
ただし、がん治療における使用は標準治療として確立されていないため、患者様には個別にリスクや効果について十分に説明を行い、ご理解と同意をいただいたうえで治療を実施いたします。
主な副作用
- 消化器系症状
- 吐き気、嘔吐
- 下痢
- 腹痛
- 肝機能障害
- 肝酵素(AST, ALT, ALP, ビリルビン)の上昇
- 神経毒性
- 一部の研究では脳幹神経毒性(高用量または長期使用時)
- 頭痛、めまい、ふらつき
- アレルギー反応
- 皮膚発疹、かゆみ
- アナフィラキシーの可能性(非常に稀)
- 心血管系への影響
- 心電図異常(QT延長)
- 低血圧(急速静注の場合)
投与経路による副作用の違い
- 経口投与:主に消化器症状、軽度の肝機能障害
- 静脈内投与:血液系の副作用、神経毒性のリスクが高まる
局所注射(腫瘍内投与):局所の炎症、痛み、発赤
「アルテミシニン誘導体」アルテスネイトでのがん治療
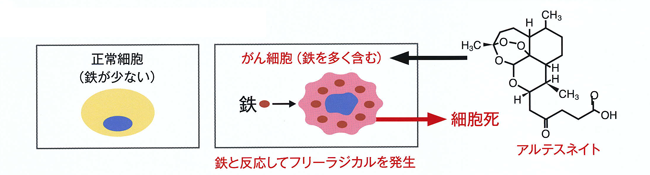
がん細胞がフリーラジカルに弱い特性を利用
がん細胞は、トランスフェリンレセプターを介したメカニズムにより、鉄を多く取り込んでいます。
つまりがん細胞内には鉄イオンが多く含まれているのですが、アルテスネイトはその鉄イオンと反応して、フリーラジカルを発生します。
一般にフリーラジカルはがんを発生させる原因とされますが、一方でがん細胞自体がフリーラジカルに弱いことも知られています。
そのためアルテスネイトが投与されると、がん細胞が選択的に障害を受け、消滅するのです。
以上のことから、アルテスネイトを投与する前に鉄を投与して、がん細胞内の鉄の量を増やしておくと、抗腫瘍作用を増強することができます。
がん細胞内に鉄が多くあるのに比べ、正常細胞はあまり鉄を含んでいません。
したがってアルテスネイトは、がん細胞に比較的特異的に細胞障害作用を示します。
加えて、正常細胞にはSODやカタラーゼ、グルタチオン・ペルオキシダーゼといったフリーラジカルの害を消す抗酸化酵素が含まれていますが、 がん細胞にはそれらがほとんど含まれていないため、がん細胞だけが消滅することになるわけです。
注意:アルテミシニン誘導体は、国内で医薬品医療機器等法に基づく承認を受けていない未承認医薬品です。
また、がん治療において標準治療として確立されたものではありません。
入手経路と安全性
「アルテミシニン誘導体は、信頼性の高い供給元を通じて適切に入手しています。
治療に使用する薬剤は、品質管理が徹底されたものを用いております。
また、安全性については、抗マラリア薬として世界中で広く使用されている実績があり、国際的なデータに基づいて確認されています。
ただし、がん治療における長期的な安全性や有効性については、十分なエビデンスが確立されていない点をご理解ください。
多彩な抗がん作用
アルテスネイトの抗腫瘍作用のメカニズムは、がん細胞内でフリーラジカルの産生を増やし、酸化ストレスを高めて、がん細胞に細胞死(アポトーシスや壊死)を引き起こすのが基本です。
さらに、腫瘍組織の血管新生を阻害する作用、細胞外の結合組織を分解する酵素の活性を阻害することによってがん細胞の転移と浸潤を抑制する作用、トポイソメラーゼⅡα阻害作用や 細胞内シグナル伝達系に作用してアポトーシスを誘導する作用など、多彩な抗がん作用が報告されています。
アルテミシニン誘導体アルテスネイト
誘導体(ゆうどうたい、英:derivative)は、有機化学の用語のひとつで、ある有機化合物を母体として考えたとき、 官能基の導入、酸化、還元、原子の置き換えなど、母体の構造や性質を大幅に変えない程度の改変がなされた化合物のこと。
アルテスネイトの抗がん作用のしくみ
正常細胞とがん細胞の比較
| 正常細胞 | がん細胞 | |
| 細胞内の抗酸化酵素量 (フリーラジカルから細胞を守るSODやカタラーゼやグルタチオン・ペルオキシダーゼ等の酵素量) | 多い | 非常に少ない |
| 細胞内の鉄分含有量 | 少ない | 非常に多い |
| 酸化ストレスによる細胞障害 (アルテスネイトが鉄と反応してフリーラジカルを産生した際の細胞障害度) | 少ない | 非常に多い |
正常細胞とがん細胞の比較
| 細胞内の抗酸化酵素量 (フリーラジカルから細胞を守るSODやカタラーゼやグルタチオン・ペルオキシダーゼ等の酵素量) | |
| 正常細胞 | 多い |
| がん細胞 | 非常に少ない |
| 細胞内の鉄分含有量 | |
| 正常細胞 | 少ない |
| がん細胞 | 非常に多い |
| 酸化ストレスによる細胞障害 (アルテスネイトが鉄と反応してフリーラジカルを産生した際の細胞障害度) | |
| 正常細胞 | 少ない |
| がん細胞 | 非常に多い |
がんにおけるアルテミシニンの使用に関連する研究
非小細胞肺癌(NSCLC)患者におけるアルテスネイトの影響
中国のDongguanKuanghua Hospitalの研究者が行った研究では、アルテスネイト(アルテミシニンの誘導体)とNP(ビノレルビンとシスプラチンの化学療法レジメン) およびNP単独の120例の治療における有効性と毒性を比較しました。進行した非小細胞肺がん(NSCLC)。
(Zhu-Yi Zhang et al、Zhong Xi Yi Jie He Xue Bao。、2008)
NP化学療法レジメンのみを受けた患者と比較して、アルテスネイトとNP化学療法を併用した患者では、短期生存率が34.5%から45.1%にわずかに増加し、 平均生存期間が45週間から44週間にわずかに減少しました。
1年生存率が32.7%から45.1%にわずかに増加しました。
この研究では、アルテミシニンと化学療法レジメンの両方を受けた患者の疾病管理率は88.2%であり、化学療法のみを受けた患者よりもわずかに高い72.7%であることがわかりました。
この研究では、XNUMXつのグループ間で毒性(骨髄抑制と消化反応)に有意差は見られませんでした。
全体として、この研究では、アルテスネートと化学療法の組み合わせで治療された患者は、化学療法と一緒にアルテスネイトを投与されなかった患者よりも癌の進行が遅いため、 アルテスネイトがNSCLCの治療に有益である可能性があることがわかりました。
進行性固形腫瘍悪性腫瘍患者におけるアルテスネート静脈内投与の影響
バージニア州のイノバヘルスシステム、ワシントンDCのジョージタウン大学メディカルセンター、および米国ノースカロライナ州のカロライナヘルスケアシステムは、 進行性固形がんの19人の患者を対象に第I相試験を実施し、静脈内アルテスネート(アルテミシニンの誘導体)。
(John F Deeken et al、Cancer Chemother Pharmacol。、2018)
これら19人の癌患者で行われた研究に基づいて、静脈内アルテスネイト/アルテミシニンの最大耐量は18mg / kgであることがわかりました。
研究者らはまた、治療は十分に許容されたと結論付けましたが、この前治療された集団では中程度の臨床活動しか見られませんでした。
結腸直腸癌患者における経口アルテスネート療法の影響
ロンドン大学の感染免疫研究所と英国のイーストサリー病院、ドイツのヨハネスグーテンベルク大学とUniversitätsklinikumTübingen、ベルギーのダフラファーマの研究者によって行われた臨床研究で、 研究者は抗癌を評価しました20人の結腸直腸癌患者における経口アルテスネイト(アルテミシニンの誘導体)の効果と忍容性。(Sanjeev Krishna et al、EBioMedicine。、2014)
9人の結腸直腸癌患者は経口アルテスネイトを与えられ、11人の患者は手術前にプラセボを与えられました。
この研究では、アルテスネイトを投与されたグループの患者の12%が、プラセボグループと比較して細胞の7%を超えるアポトーシスを示したことがわかりました。
この研究では、平均42か月の追跡期間中に、アルテスネイトを投与された1人の患者とプラセボを投与された6人の患者が再発性結腸直腸癌を発症したこともわかりました。
研究者らは、アルテスネイトは結腸直腸癌においてアポトーシスおよび抗増殖特性を有する可能性があり、十分に許容される可能性があると結論付けました。
転移性ブドウ膜黒色腫におけるアルテスネートの影響
ドイツのエアランゲン大学病院の研究者は、転移性ブドウ膜黒色腫患者における標準的な化学療法と組み合わせたアルテスネイト(アルテミシニンの誘導体)の影響を評価しました。
この研究は、標準的な化学療法のみによって引き起こされるもの以外の追加の副作用がなく、治療計画が十分に許容されることを強調しました。(Thomas G Berger et al、Oncol Rep。、2005)
さらに、彼らは、XNUMX番目の薬剤と組み合わせて服用した場合のアルテスネイトがブドウ膜黒色腫患者に有望であることがわかったと述べました。
彼らはそれを見つけました
- アルテスネイトを投与された患者のXNUMX人は、フォテムスチンと呼ばれる薬と一緒に服用したときに一時的な反応を経験しました。
- 47番目の患者は、2番目の薬剤であるダカルバジンと一緒にアルテスネイトを投与された後、 疾患の安定化と脾臓および肺転移の減少を示し、IV期ブドウ膜黒色腫の最初の診断から5か月後に生存しました。
進行子宮頸癌における経口アルテミシニン-R /アルテミシニン誘導体の影響
ベルギーのDafraPharma Ltdの研究者は、進行性子宮頸癌の10人の患者を対象にArtenimol-R(アルテミシニンの誘導体)を28日間経口投与することの臨床的利点と安全性を評価しました。
この研究では、10人の患者全員が寛解し、痛みや膣分泌物などの症状が平均7日間で消えたことがわかりました。(Frans Herwig Jansen et al、Anticancer Res。、2011)
アドオン療法としてアルテスネートで治療された転移性 または局所進行性乳がん患者の聴器毒性
聴器毒性は、アルテスネiト(アルテミシニンの誘導体)療法の長期的な毎日の投与で治療された乳がん患者の潜在的な安全上の懸念である可能性があります。
したがって、ドイツのハイデルベルクにあるさまざまな施設の研究者が、進行性乳がん患者33人を対象にアルテスネイトの安全性と忍容性を評価するために、ARTIC M2 / 23試験と呼ばれる前向き第I相用量漸増試験を実施しました。 (MiriamKönigetal、Cancer Chemother Pharmacol。、2016年)
研究はそれを発見しました
- 4人の患者は、おそらくアルテスネートの摂取が原因で、聴覚障害に関連する有害事象を示しましたが、治療の中断を必要としないため、これらのいずれも重篤な有害事象として分類されませんでした。
- 4人の患者が試験段階でめまいを起こし、そのうちのXNUMX人は重篤な有害事象として分類されましたが、Artesunateの中止後に可逆的でした。
転移性乳がん患者における経口アルテスネートの影響
ドイツのハイデルベルクにあるさまざまな機関の研究者によって行われた同じオープンフェーズI試験(ARTIC M33 / 2)は、 転移性乳がん患者を対象としたアルテスネイト(アルテミシニンの誘導体)による長期治療の安全性と忍容性を評価しました。彼らの癌治療を受けています。
この研究では、転移性乳がんの13人の患者において、最大200治療月で最大2.3 mg /日のアルテスネイト経口追加療法(4.1-37 mg / kg BW /日)は大きな安全上の懸念をもたらさなかったと述べています。
(Cornelia von Hagens et al、Phytomedicine。、2019)
結論
目立った副作用など見られず使いやすい薬剤ですのでがん治療や新型コロナ感染症の重症化予防などにお役立てください。



